电化学腐蚀中的阴极反应与阳极反应
2019-4-28 19:16:36点击:
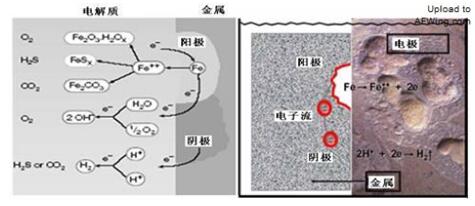
电化学腐蚀是指金属表面与离子导电的介质(电解质)发生电化学反应而引起的破坏。电化学机理进行的腐蚀反应包含一个阳极反应和一个阴极反应,并以金属内部的电子流和介质中的离子流形成电流回路。阳极发生氧化反应,即金属离子从金属转移到介质中,并将电子留在金属上:阴极发生还原反应,即介质中的氧化剂吸收来自阳极的电子。

例如,碳钢在酸中的腐蚀,在阳极区铁被氧化为Fe2+离子,所放出的电子由阳极(Fe)流至阴极(钢中的渗碳体Fe,C)上被H*离子吸收而还原成氢气,即
阳极反应: Fe→Fe2++2e阴极反应: 2H++2e→H2↑
总反应: Fe+2H+→Fe2++H2↑
可见,与化学腐蚀不同,电化学腐蚀的特点在于它的腐蚀过程可分为两个相对独立并可同时进行的过程。在腐蚀的金属表面上,由于存在着在空间或时间上分开的阳极区和阴极区,腐蚀反应过程中微量电子从阳极区传递到阴极区,产生微电流。
- 上一篇:防止金属腐蚀的方法有哪些? 2019/4/30
- 下一篇:什么是化学腐蚀? 2019/4/25
